Медицинские изделия
Медицинские изделия - любые инструменты, аппараты, приборы, оборудование, материалы и прочие изделия, применяемые в медицинских целях отдельно или в сочетании между собой, а также вместе с другими принадлежностями, необходимыми для применения указанных изделий по назначению, включая специальное программное обеспечение, и предназначенные производителем для профилактики, диагностики, лечения и медицинской реабилитации заболеваний, мониторинга состояния организма человека, проведения медицинских исследований, восстановления, замещения, изменения анатомической структуры или физиологических функций организма, предотвращения или прерывания беременности, функциональное назначение которых не реализуется путем фармакологического, иммунологического, генетического или метаболического воздействия на организм человека.
Классы риска медицинских изделий
При классификации медицинских изделий каждое медицинское изделие может быть отнесено только к одному классу:
- класс 1 - медицинские изделия с низкой степенью риска;
- класс 2а - медицинские изделия со средней степенью риска;
- класс 2б - медицинские изделия с повышенной степенью риска;
- класс 3 - медицинские изделия с высокой степенью риска.
При классификации медицинских изделий учитывают их функциональное назначение и условия применения, а также следующие критерии:
- Принадлежность к изделиям для диагностики in vitro
- Количество контактирующих с пациентом материалов
- длительность применения медицинских изделий;
- инвазивность медицинских изделий;
- наличие контакта медицинских изделий с человеческим телом или взаимосвязи с ним;
- способ введения медицинских изделий в тело человека (через анатомические полости или хирургическим путем);
- применение медицинских изделий для жизненно важных органов и систем (сердце, центральная система кровообращения, центральная нервная система);
- применение источников энергии.

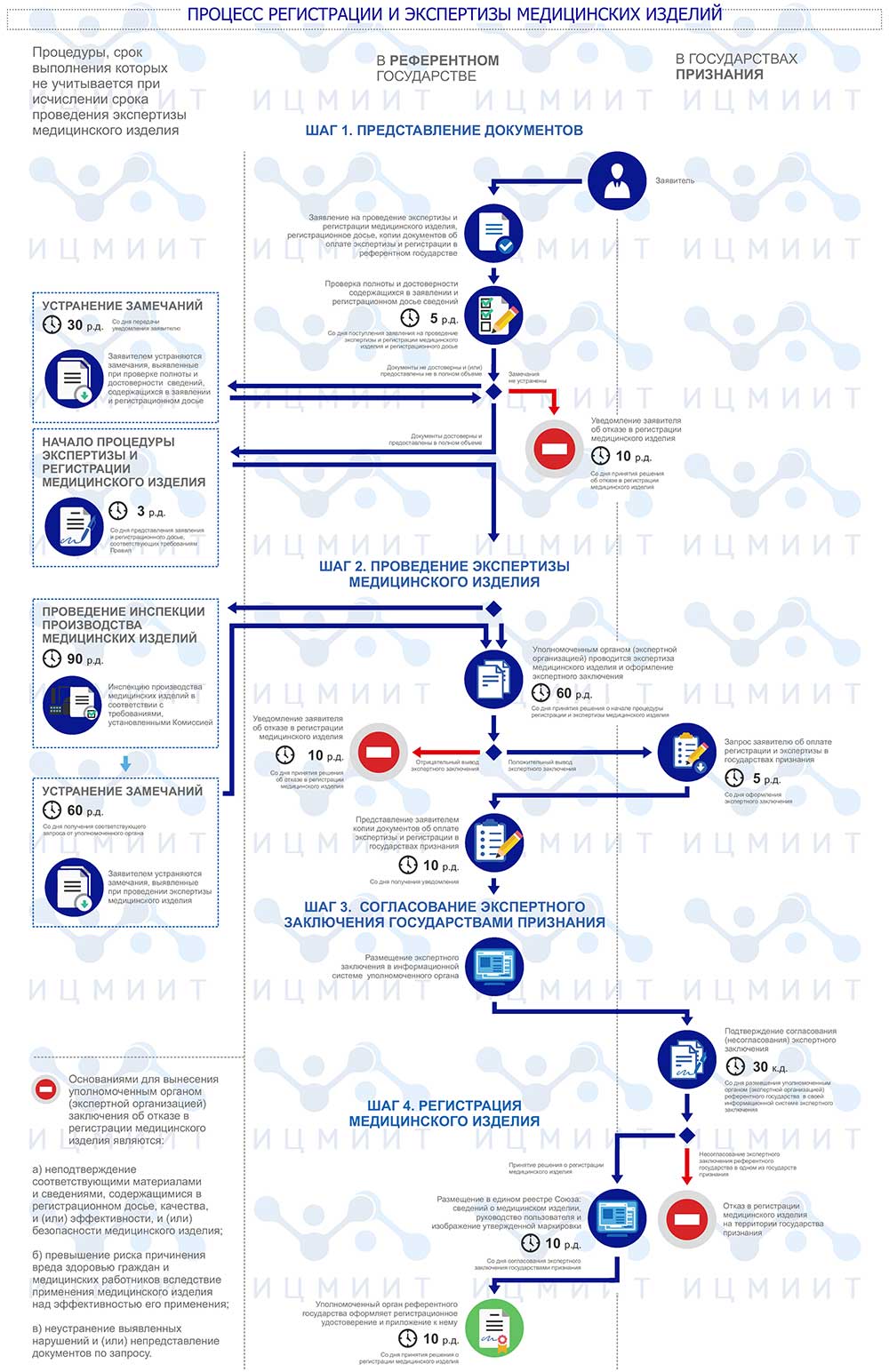
Регистрация медицинских изделий в рамках ЕАЭС
С 1 января 2015 года Россия входит в Евразийский экономический союз (ЕАЭС), государствами-членами которого, на данный момент, так же являются Республика Армения (с 2015 г.), Республика Беларусь (с 2015 г.), Республика Казахстан (с 2015 г.) и Кыргызская Республика (с 2015 г.). Главное преимущество для производителей медицинских изделий в принадлежности к ЕАЭС заключается в однократной регистрации (в любом из государств-членов ЕАЭС) и последующей возможности реализации своих изделий как медицинских в странах-признания ЕАЭС
Уже сейчас регистрация медицинских изделий в рамках ЕАЭС осуществляется в соответствии с Правилами регистрации и экспертизы безопасности, качества и эффективности медицинских изделий, утвержденными Решением Совета ЕАЭС от 12.02.2016 № 46. В настоящее время и по 31 декабря 2021 г. длится переходный период, позволяющий производителям медизделий подготовиться к грядущим изменениям и оформить регистрационные удостоверения на их изделия (действующие РУ, в т.ч. бессрочные, прекратят своё действие 31 декабря 2021 г.).
Регистрация мед. изделий является обязательной, т.к. одна из обязанностей надзирающих органов государств-членов – наблюдение за качеством и безопасностью медицинских товаров, которые продаются на рынке ЕАЭС. В обращение может поступить только та продукция, которая прошла обязательную регистрацию.
Самостоятельно разобраться во всех тонкостях действующего законодательства затруднительно даже для опытных специалистов, но уже сейчас для обращения медизделий на территории России (а в будущем – и на территории ЕАЭС) производителям доступна регистрация медизделий экспертами нашего инженерного центра, в соответствии со всеми актуальными требованиями, в т.ч. по Правилам ЕАЭС.
Нормативная база
- Постановление Правительства Российской Федерации от 30.11.2024 № 1684 "Об утверждении Правил государственной регистрации медицинских изделий"
- Приказ Министерства здравоохранения Российской Федерации от 11.04.2025 № 181н "Об утверждении требований к содержанию технической и эксплуатационной документации производителя (изготовителя) медицинского изделия"
- Федеральный закон от 21.11.2011 № 323-ФЗ об основах охраны здоровья граждан в РФ, Статья 38 «Об основах охраны здоровья граждан в РФ»
- Приказ Министерства здравоохранения Российской Федерации от 20.03.2020 № 206н "Об утверждении Порядка организации и проведения экспертизы качества, эффективности и безопасности медицинских изделий"
- Постановление Правительства РФ от 03.04.2020 № 430 "Об особенностях обращения медицинских изделий, в том числе государственной регистрации серии (партии) медицинского изделия"
- Приказ Минздрава России от 16.05.2013 N 300н "Об утверждении требований к медицинским организациям, проводящим клинические испытания медицинских изделий, и порядка установления соответствия медицинских организаций этим требованиям"
- Решение Совета Евразийской экономической комиссии от 12.02.2016 № 46 «О Правилах регистрации и экспертизы безопасности, качества и эффективности медицинских изделий»
- Приказ Минздрава России от 29.04.2025 № 257н «Об утверждении перечня медицинских изделий, относящихся к средствам измерений в сфере государственного регулирования обеспечения единства измерений, и порядка проведения их испытаний в целях утверждения типа средств измерений»
Задайте вопрос здесь
Наш специалист ответит Вам в течение рабочего дня